Алгоритмы заряда Ni-MH. Какой способ "лучше"? Как не проскочить -∆V?

Ni-MH давно вышел из моды. «Давно» — это несколько лет назад. И далеко не везде и не для всех.
Несмотря на местами вполне обоснованную критику со стороны продвинутых пользователей разномастного «лития» в мире до сих пор используется огромное количество устройств на Ni-MH «тяге». Скорее всего, речь идет о сотнях миллионов или нескольких миллиардах (ИМХО). От мультиметров, тонометров и мышек до елочных гирлянд, электрических игрушек и прочей бытовухи.
Так что, пока с этим самым морально устаревшим Ni-MH надо как-то жить и как-то бороться с главной проблемой никель-металлгидрида — отсутствием вменяемого алгоритма заряда оного.
Как гарантированно зарядить Ni-MH от 0 до 100% и полностью исключить вредное явление перезаряда? Строго говоря — почти никак. Но заметно сгладить негативные моменты сего действа в принципе возможно при комплексном подходе с применением дополнительных алгоритмов определения момента окончания заряда.
Под катом — экскурс в электрохимию Ni-MH и наглядная демонстрация практического применения «самого продвинутого» метода "-dv/dt" или «минус дельта». Великих открытий там нет, но может кого-то заинтересуют некоторые моменты.
[Если содержание данного раздела вдруг стало совсем непонятно, то придется все это дело пропустить. Мало чего потеряете, только полная ясность понимания некоторых моментов во 2 разделе не так что бы гарантирована.]
Рассмотрим основные электрохимические (ЭХ) процессы, протекающие при заряде Ni-MH ячейки. Таких процессов три:
☀ Основной заряд (Ni⁺²→Ni⁺³)&(М → МН), т.н. фарадеевский процесс
☀☀ Кислородный цикл
☀☀☀ Переразряд на никелевом электроде Ni⁺³ → Ni⁺⁴
При заряде от 0 до 100% эти процессы протекают всегда и они протекают параллельно. Это конкурирующие реакции. При этом они забирают некоторую долю эл. энергии, подводимой извне. Если добавить неизбежное тепловое рассеяние по Джоулю-Ленцу и не учитывать маловероятные побочные процессы, то получаем полный энергетический баланс:
E(от внешнего источника)=E(основной процесс)+E(кислородный и цикл)+E(Ni⁺³→Ni⁺⁴)+E(джоулево тепло).
Но интенсивности протекания на разных этапах заряда три химических процесса часто сильно отличаются. Поэтому в ряде случаев наличием того или иного процесса можно пренебречь (скорость → 0).
► Так, на начальной стадии заряда до 70-80% DoC***, основной (фарадеевский) процесс (Ni⁺²→Ni⁺³)&(М → МН) является фактически единственным химическим процессом в системе. При этом вся подводимая энергия расходуется на протекание основного процесса и диссипацию в виде джоулева тепла.
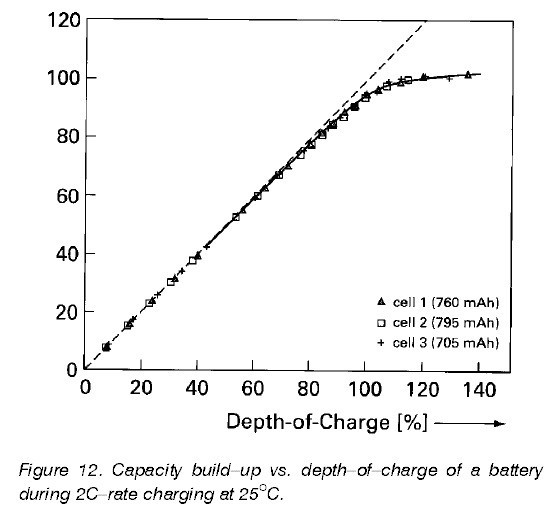 ***Примечание. DoC (Depth of Charge) переводится как «глубина заряда» ячейки или аккумуляторной батареи. Определяется как отношение количества израсходованного электричества при заряде к заявленной (или реальной) емкости. К истинной глубине заряда аккумулятора имеет весьма опосредованное отношение, т.к. часть эл. энергии неизбежно тратится впустую.
***Примечание. DoC (Depth of Charge) переводится как «глубина заряда» ячейки или аккумуляторной батареи. Определяется как отношение количества израсходованного электричества при заряде к заявленной (или реальной) емкости. К истинной глубине заряда аккумулятора имеет весьма опосредованное отношение, т.к. часть эл. энергии неизбежно тратится впустую.
Поэтому существует принципиальная возможность сверхбыстрого заряда батарей Ni-MH токами 5-10С до половины или 2/3 емкости. При наличии эффективной системы охлаждения и термоконтроля каждой ячейке в сборке. Но о практической реализации таких проектов я не слышал. В отличии от промышленных батарей Ni-Cd.
► В интервале DoC (Depth of Charge) 70-100% происходит смена преобладающего процесса, потребляющего подводимую энергию с основного (фарадеевского) на кислородный цикл. Кислородный цикл экзотермичен.
►После 95-100%, особенно при больших плотностях тока становится заметным и переразряд (Ni⁺³ → Ni⁺⁴), так же как кислородный цикл идущий с выделением тепла. Потому что переразряд — это тоже цикл (Ni⁺³ ⇆ Ni⁺⁴), но с более медленной диссипацией энергии.
Какие же факторы оказывают влияние на интенсивность протекания трех конкурирующих процессов?
• Уровень заряда ячейки
• Сила тока, протекающего через ячейку
• Температура и давление О₂ в системе
Насчет силы тока — тут есть некоторое лукавство. Ибо сила тока, протекающего через ячейку зависит от величины напряжения, приложенного к ячейке. И именно эта величина оказывает непосредственное влияние на интенсивность протекания ЭХ процессов. Но ЗУ (зарядное устройство) задает именно значение силы тока, а автоматика подбирает нужную разность потенциалов на электродах. Поэтому логичнее оперировать параметром «сила тока».
[В качестве исходника для данного раздела взята статья известного фонаревщика датчанина HKJ и заметно переработана: опущено малосущественное, добавлено недостающее (ИМХО).]
Надежного критерия окончания заряда не существует. Поэтому таких способов напридумано множество. И в интернетах говорено о них много раз. Одно плохо — практически все знают что происходит с напряжением и температурой в процессе заряда, но не понимают почему это происходит. Ибо химический источник тока для человека, не замутненного электрохимией, по сути «черный ящик» или «вещь в себе» (Кант).
Но мы, вооружившись материалом из разд.1, попробуем разобраться.
Особое внимание будет уделено методу "-∆V", а про все остальные — вскользь.
Про «древний» и «сверхмедленный» заряд «никелевых» ячеек (Ni-Cd и Ni-MH) многие слышали. Заряд током 0.1С, отсечка по времени через 14-16 часов.
Но самое интересное, что этот способ заряда самый надежный и наименее вредный для потрохов аккумулятора. Перезаряд (в химическом понимании) там присутствует, но он ничтожно мал. Почему? Идея проста: за первые 7-8 часов элемент набирает 70-80% номинальной емкости. Потом начинает заметно протекать кислородный цикл, который чем дальше, тем больше пожирает подводимое электричество. Тем не менее, элемент за оставшиеся 6-8 час. неспешно добирает оставшуюся емкость до фактической максимальной. Ввиду малости зарядного тока переразряд на никелевом электроде (Ni⁺³ → Ni⁺⁴) стремится к нулю и его можно не учитывать.
Теперь становиться понятным почему в рекомендациях МЭК (калька с английского — ГОСТы) на протяжении многих лет присутствует один интересный момент
ссылка
 В подавляющем большинстве современных ЗУ Low current charging отсутствует, он там не нужен. В SkyRC MC3000 — есть. Исключительно для проверки по ГОСТу.
В подавляющем большинстве современных ЗУ Low current charging отсутствует, он там не нужен. В SkyRC MC3000 — есть. Исключительно для проверки по ГОСТу.
Метод прост как трусы. При постоянном токе заряжаем до момента, пока напряжение не достигнет определенного значения.
Используется во многих недорогих ЗУ. Самый известный пример — Lii-500. ТУТ обзор от датчанина HKJ.
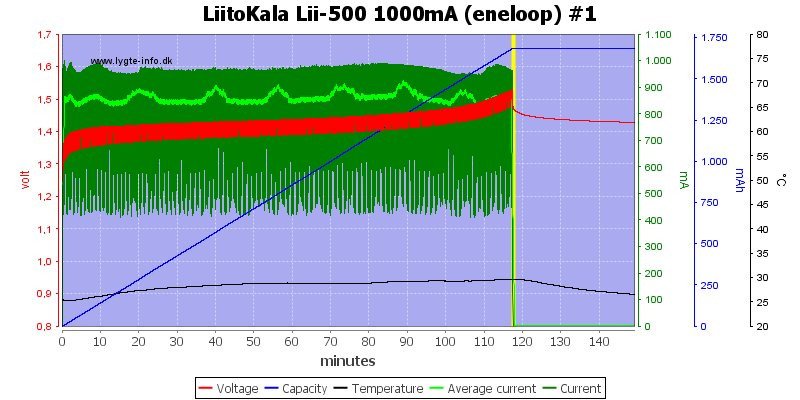 Рекомендуется замерять разность потенциалов на электродах при кратковременном снятии нагрузки, т.е. НРЦ (напряжение разорванной цепи). Так получается точнее.
Рекомендуется замерять разность потенциалов на электродах при кратковременном снятии нагрузки, т.е. НРЦ (напряжение разорванной цепи). Так получается точнее.
Проблемой данного метода является то, что измеренное значение НРЦ зависит от температуры и скорости заряда (поляризация электродов, которая не может рассосаться мгновенно), что создает дополнительные головняки.
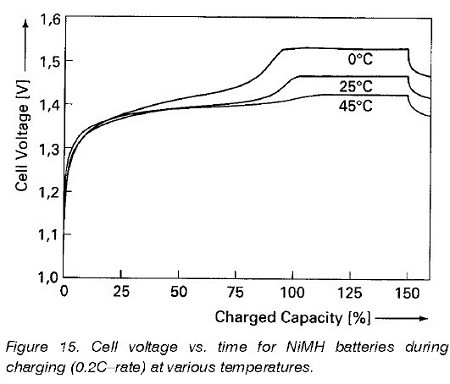 Триггерное значение НРЦ производителями ЗУ подбирается в предположении температуры 20-30°С. Если заряд производится в шибко холодном помещении и на малых токах, то весьма вероятен заметный недозаряд. Но еще хуже, если все это происходит на жаре и при больших токах без принудительного охлаждения — возможно не выполнение условия остановки процесса и «бесконечный» заряд.
Триггерное значение НРЦ производителями ЗУ подбирается в предположении температуры 20-30°С. Если заряд производится в шибко холодном помещении и на малых токах, то весьма вероятен заметный недозаряд. Но еще хуже, если все это происходит на жаре и при больших токах без принудительного охлаждения — возможно не выполнение условия остановки процесса и «бесконечный» заряд.
Нынешние продвинутые ЗУ часто определяют момент окончания заряда Ni-MH/Ni-Cd по критерию "- ∆V". Кратковременное снижение разности потенциалов между электродами ячейки (- ∆V) происходит где-то вблизи окончания заполнения ячейки. Но какова природа наблюдаемого — ∆V?
Предположительно, происходит следующее.
1) Как уже было отмечено, чем ближе ячейка к состоянию полного заряда, тем более вяло протекает основной процесс (Ni⁺²→Ni⁺³)&(М → МН) и сильнее выражен кислородный цикл. Активное протекание кислородного цикла приводит к тому, что бОльшая часть подводимой эл. энергии превращается в тепло. Если бы не перезаряд Ni⁺³ → Ni⁺⁴, то при уровне заряда ячейки 100% в тепло превращалась бы вся энергия (кислородный цикл + джоулево тепло).
2) Итак, при приближении ячейки к состоянию полного заряда наблюдается резкий рост Т. Что приводит к увеличению проводимости электролита (р-р КОН)
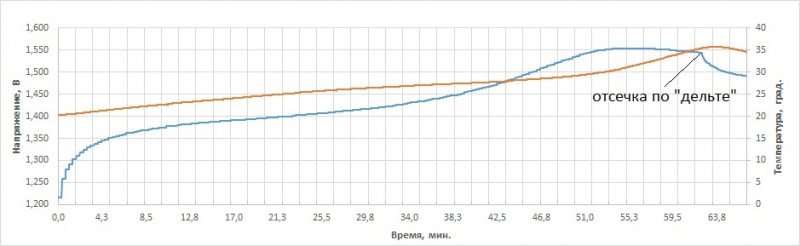
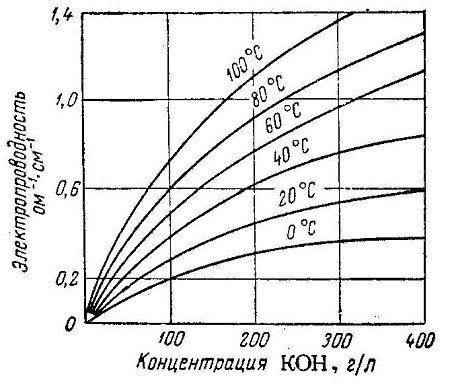 3) Для того, что бы ток, протекающий через ячейку, оставался постоянным (равным заданному) ЗРУ автоматически начинает снижать внешнюю разность потенциалов. В результате получаем горб на кривой напряжения. Правый склон того горба — это и есть «эффект -∆V» или "«минус дельты».
3) Для того, что бы ток, протекающий через ячейку, оставался постоянным (равным заданному) ЗРУ автоматически начинает снижать внешнюю разность потенциалов. В результате получаем горб на кривой напряжения. Правый склон того горба — это и есть «эффект -∆V» или "«минус дельты».
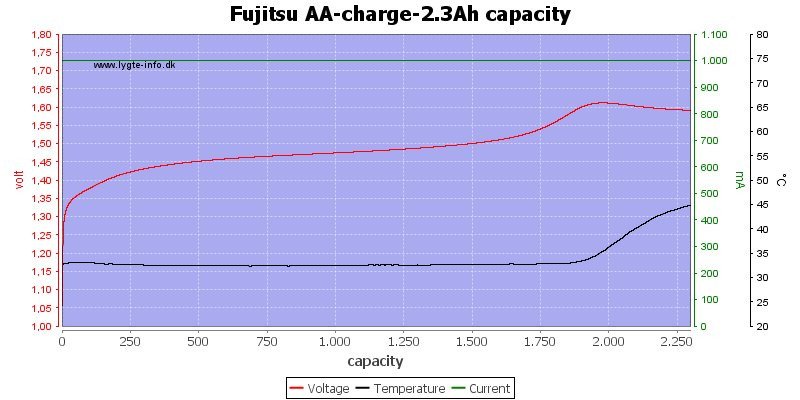
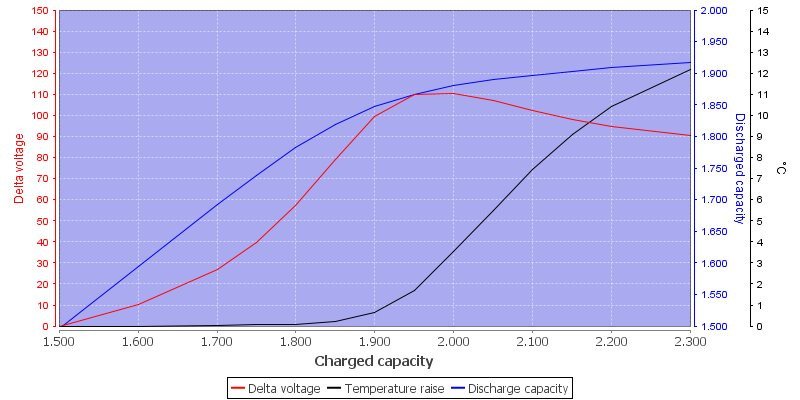 4) И опять-таки рекомендуется замерять разность потенциалов на электродах при кратковременном снятии нагрузки, т.е. НРЦ (напряжение разорванной цепи).
4) И опять-таки рекомендуется замерять разность потенциалов на электродах при кратковременном снятии нагрузки, т.е. НРЦ (напряжение разорванной цепи).
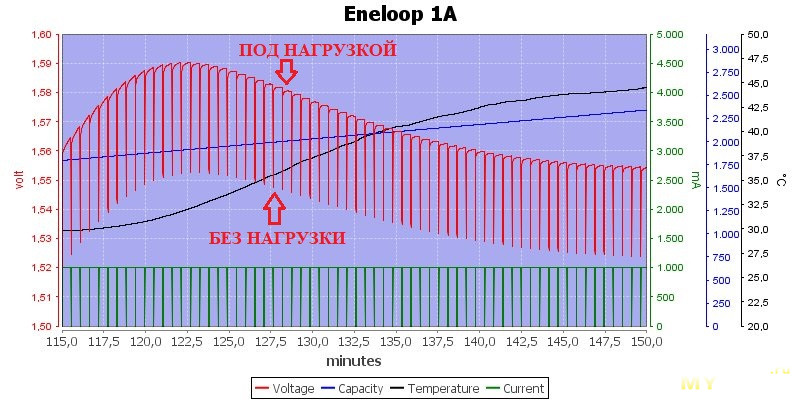 5) Чтобы достаточно надежно поймать "- ∆V" датчанин рекомендует использовать токи не ниже 0.5С. Но, как было отмечено выше, бОльшие токи заряда способствуют переокислению β-NiOOH до γ-NiOOH (или NiO₂) и ускорению деградации активной массы «никелевого» электрода.
5) Чтобы достаточно надежно поймать "- ∆V" датчанин рекомендует использовать токи не ниже 0.5С. Но, как было отмечено выше, бОльшие токи заряда способствуют переокислению β-NiOOH до γ-NiOOH (или NiO₂) и ускорению деградации активной массы «никелевого» электрода.
При малых токах зарядки эффект "- ∆V" исчезает. Вместо того чтобы искать падение напряжения, можно искать стабильное напряжение (или даже очень медленно растущее напряжение) и использовать его в качестве критерия окончания зарядки.
Метод несколько стремен в реализации и обычно используется как дополнение к "- ∆V", ежели та самая «дельта» по каким-то причинам не была «поймана».
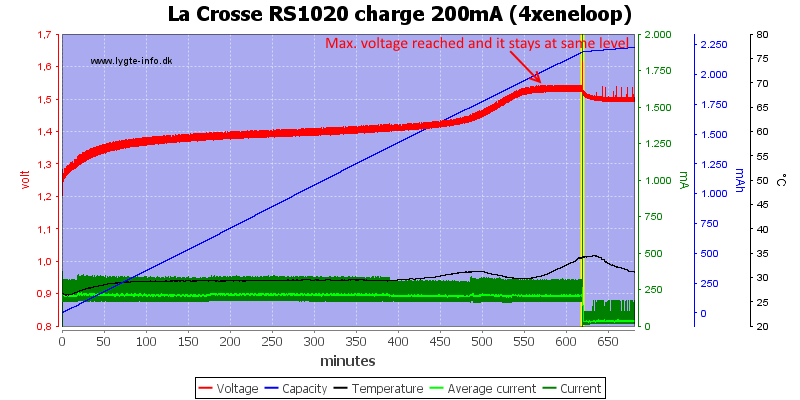
~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~
Для опытов было выбрано четыре БУ-шных аккумулятора ААА:
EN-1 и EN-2
Panasonic Eneloop BK-4MCCE даташит
FU-1 и FU-2
Fujitsu HR-4UTC даташит (дубль)
Все они сделаны на заводе Fujitsu (FDK) по одной и той же технологии и отличаются только наклейками.
 Поэтому и [краткие] даташиты у них фактически одинаковы.
Поэтому и [краткие] даташиты у них фактически одинаковы.
Давайте разберемся что там понаписано и нарисовано.
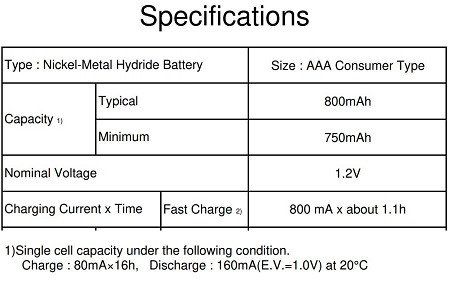 Т.н. «ёмкость» акку заявлена в двух вариантах:
Т.н. «ёмкость» акку заявлена в двух вариантах:
— минимальная (750 мАч)
— типичная (800 мАч)
Прикол в следующем — до 2011 г. производители (или вендоры) аккумуляторов могли заявлять для них ёмкость «как они ее видят» и указывать оную прямо на наклейке.
Но в IEC 61951-2:2011 МЭК обязал дополнительно указывать на наклейке минимально гарантированную ёмкость, хотя бы мелким шрифтом.
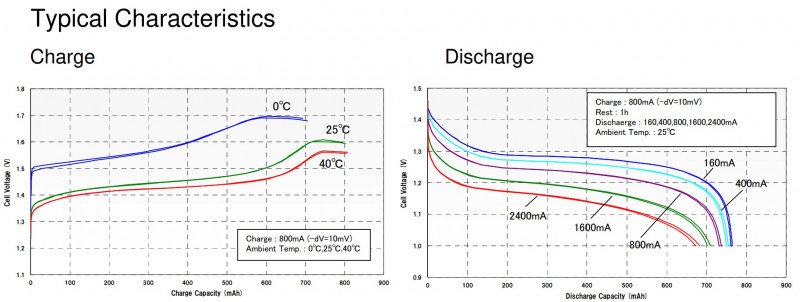 На картинках заряда и разряда показано, что заряд ячеек производится током 800мА, а критерием завершения заряда является ∆V=-10мВ. Вот от этого и будем далее танцевать.
На картинках заряда и разряда показано, что заряд ячеек производится током 800мА, а критерием завершения заряда является ∆V=-10мВ. Вот от этого и будем далее танцевать.
В опытах использовалась известное ЗРУ SkyRC MC3000. Для Ni-MH оно позволяет выставить значение ∆V от -3 до -20мВ. Замеры на предмет поимки ∆V производятся при кратковременном отключении нагрузки 3 раза в минуту.
Так же использовалась «родная» утилита MC3000_Monitor_V1.06, которая:
• [главное] записывает лог с интервалом 1 сек. в файл *.CSV
• [дополнительно] отображает что происходит в графическом окне
Графическая часть весьма примитивна и практически не настраивается. Имеет глюк с отображением оси времени (занижает на 3-4 мин. в течении каждого часа). Но смысл оной — дать только общее представление о происходящем.
Предварительно было проверена адекватность образцов.
5 циклов заряд (0.5А, ∆V=-3мВ) → пауза(30мин) → разряд (0.5А) → пауза (30мин).
Если нужно, нарисую табличку. Все равно, измеренные значения емкости не являются «гостовскими»: режимы заряда и разряда «неправильные» и паузы меньше часа:).
Опыты проводились единообразно: один цикл заряд-разряд.
Заряд (I(заряда), ∆V) → пауза(60мин) → разряд (0.16А до 1.00В)
I(заряда)=800...300мА
∆V=-10 или -3мВ
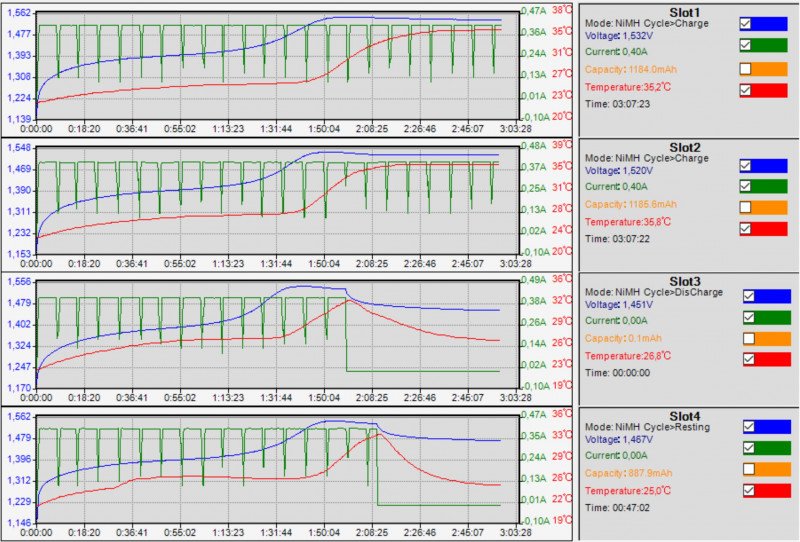
Все прошло нормально, ∆V=-10мВ зафиксирована для всех 4 образцов. Интересно, что максимум температуры всегда наблюдается чуть позже момента остановки заряда.
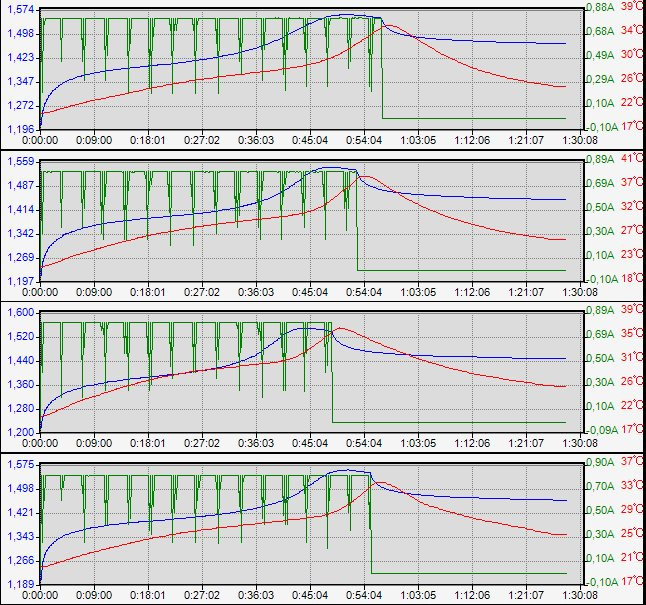 Чуть подробнее на основании лога (в качесте примера — EN-1)
Чуть подробнее на основании лога (в качесте примера — EN-1)
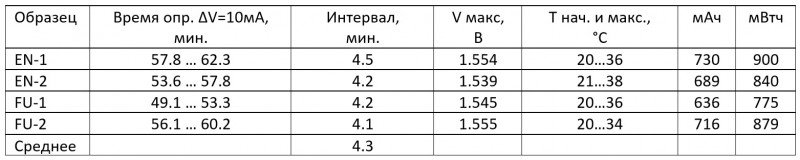
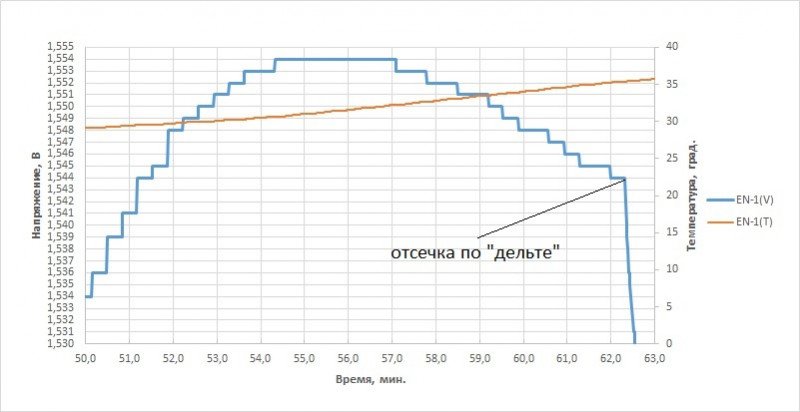 Краткая сводка:
Краткая сводка:
И опять ∆V=-10мВ зафиксирована для всех 4 образцов.
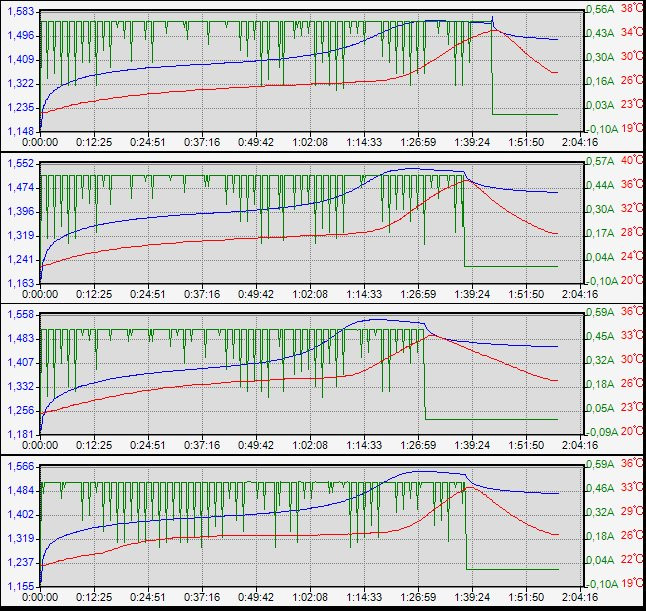 Краткая сводка:
Краткая сводка:
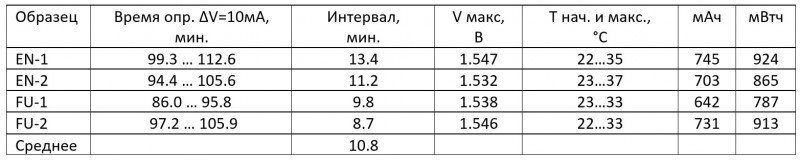
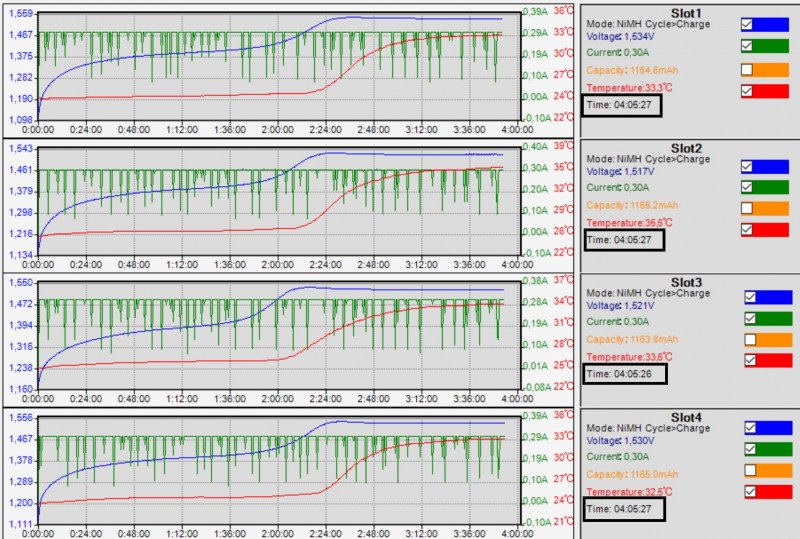
«Дельта» НЕ зафиксирована для всех 4 образцов. Хотя ждал чуть более 4 часов. На графиках время занижено, это глюк граф. интерфейса утилиты (см. выше)
 Краткая сводка:
Краткая сводка:
 Причина вполне очевидна: для всех образцов реальное значение ∆V не дотянуло до -10мВ…
Причина вполне очевидна: для всех образцов реальное значение ∆V не дотянуло до -10мВ…
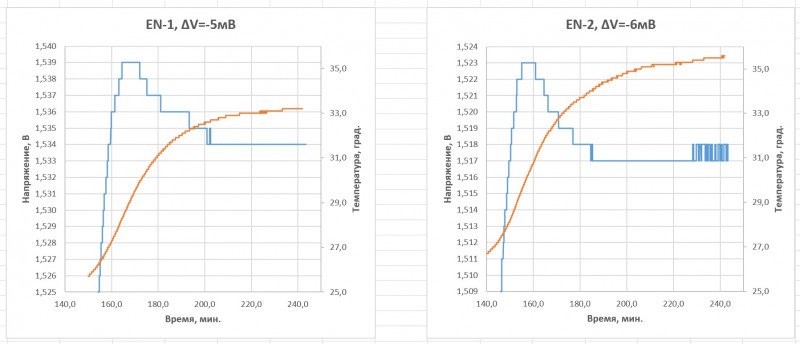
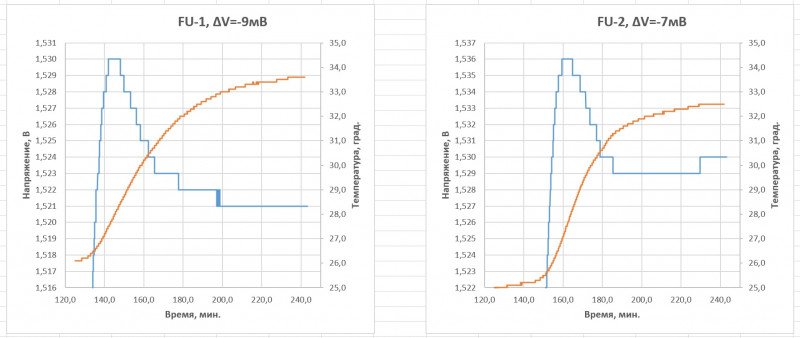 Здесь есть один нюанс: в лог записываются «верхние» значения напряжения, а определение ∆V происходит по «нижним», в моменты пауз, которые в лог не пишутся. Но ∆V по «нижним» или такая же как по «верхним» или чуть меньше.
Здесь есть один нюанс: в лог записываются «верхние» значения напряжения, а определение ∆V происходит по «нижним», в моменты пауз, которые в лог не пишутся. Но ∆V по «нижним» или такая же как по «верхним» или чуть меньше.
Что же делать в такой ситуации? Есть 2 варианта решения возникшей проблемы:
• или увеличить I(заряда)
• или уменьшить ∆V (по модулю)
Собственно, два заключительных опыта будут этому и посвящены.
Посмотрим, что получится.;)
Увы, «дельта» была «поймана» только для 2 образцов Фуджи.
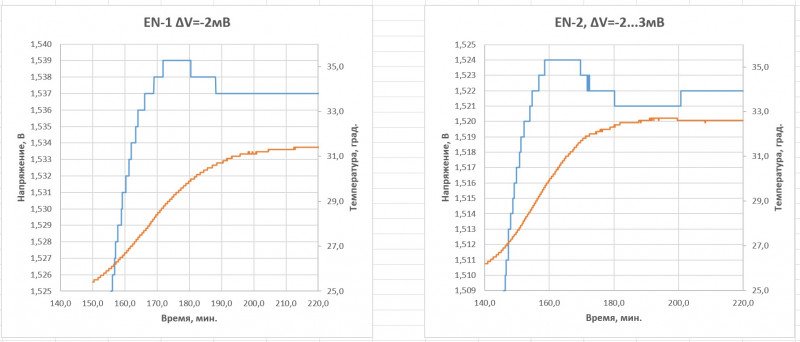
 Энелупы таки «слили», но были близки к выполнению условия по ∆V:
Энелупы таки «слили», но были близки к выполнению условия по ∆V:
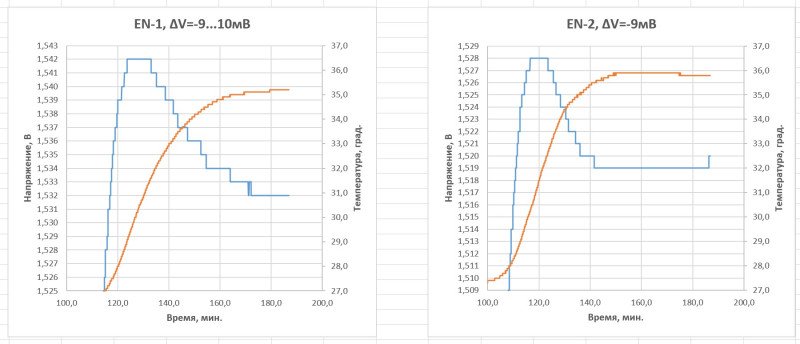 Формально, для EN-1 условие ∆V=-10 на 20 сек. было выполнено.
Формально, для EN-1 условие ∆V=-10 на 20 сек. было выполнено.
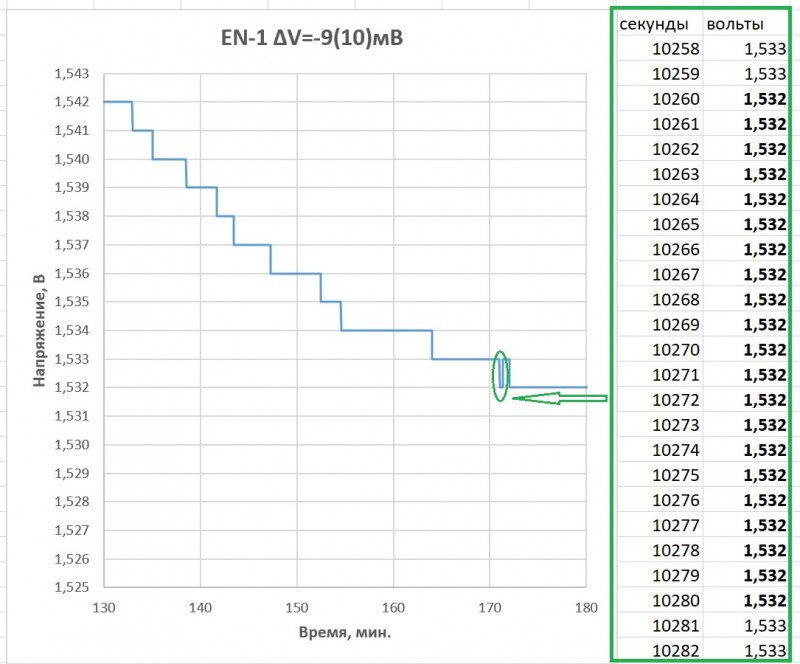 Но это для «верхних» значений напряжения (под нагрузкой). А вот для «нижних» (без нагрузки), скорее всего, нет. А именно по вторым и ловится та самая «дельта».
Но это для «верхних» значений напряжения (под нагрузкой). А вот для «нижних» (без нагрузки), скорее всего, нет. А именно по вторым и ловится та самая «дельта».
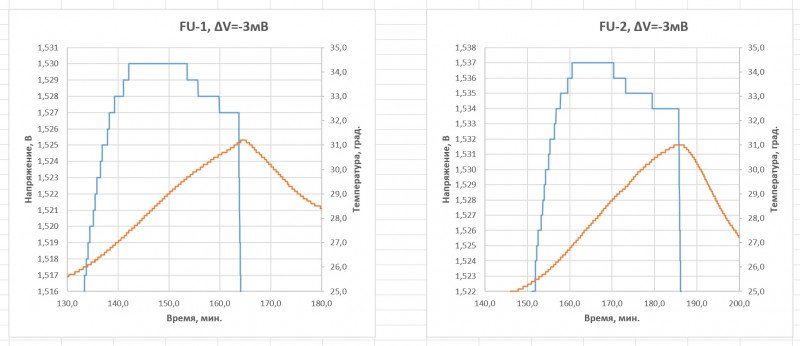
У Фуджей все хорошо:
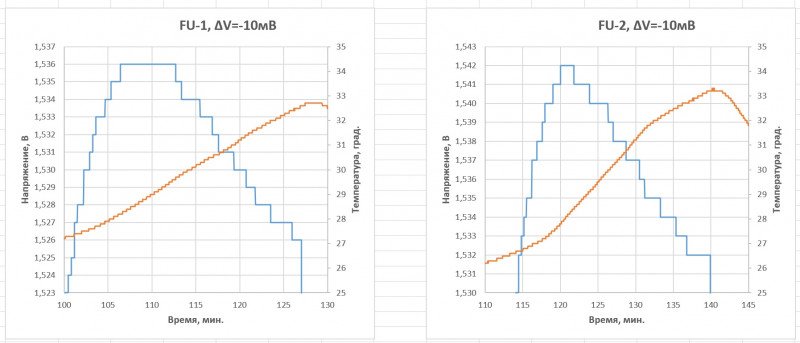
Но в результатах опыта №4 есть пока необъяснимая странность.
Посмотрите на сводную табличку и сравните чиселки, полученные для EN-2 и FU-2
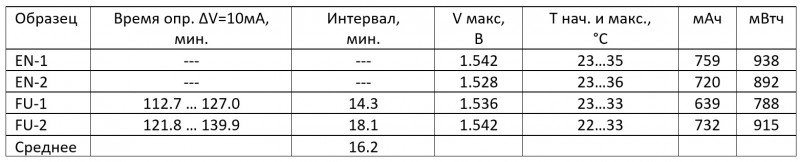 Для EN-1
Для EN-1
— меньше измеренная (текущая) емкость
— больше пиковая температура при заряде
Если я правильно понимаю, оба этих момента благоприятствуют тому, что успешная поимки «дельты» более вероятна для EN-2, а не для FU-2.
Но произошло все с точностью до наборот.
Чертовщина какая-то.
И опять «дельта» была «поймана» только для 2 образцов Фуджи....
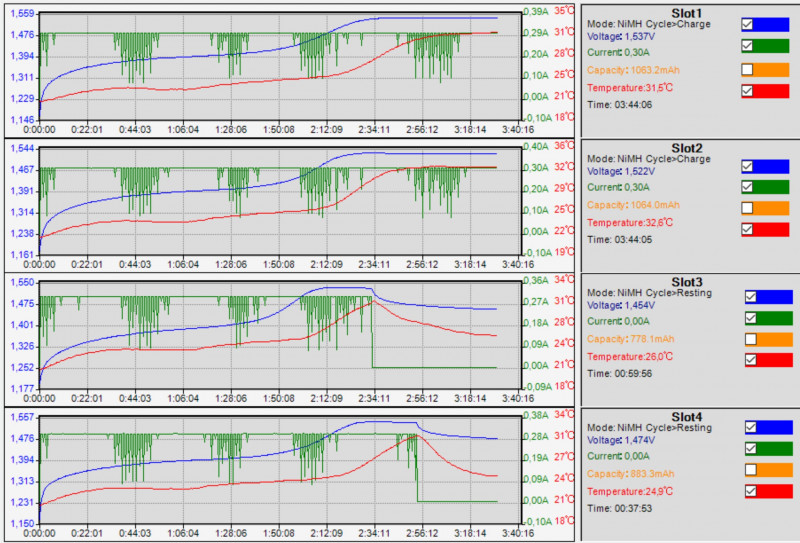
Энелупы опять «слили». Наверное, какая-то черная полоса:
А с Фуджи по-прежнему все нормально:
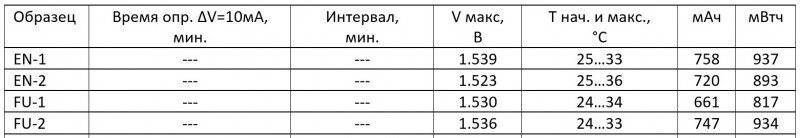
Ну и в конце — влияние I(заряда) на величины измеренных емкостей (энергоемкостей) при фиксированном значении ∆V=-10мВ. Тенденция вроде как прослеживается, но не так что бы фатальная:
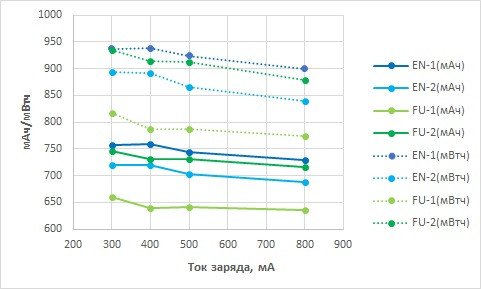 Причем, для EN-1 и EN-2 при 300 и 400 мА «дельта» не была поймана. Поэтому измеренные значения «ёмкости» для 300 и 400 мА:
Причем, для EN-1 и EN-2 при 300 и 400 мА «дельта» не была поймана. Поэтому измеренные значения «ёмкости» для 300 и 400 мА:
— фактически одинаковы;
— вполне возможно, что несколько завышены.
Вот такой он, метод "-∆V". «Самый продвинутый» и при этом самый капризный из всех ныне используемых. Ибо должно выполнится ряд условий и ЗУ в течении отлавливания «дельты» (а это не одна минута) не должно учудить вверх ни на милливольт по НРЦ во время краткосрочных пауз по нагрузке.
И что делать? Использоватьзапасные парашюты дополнительные критерии определения момента окончания заряда Ni-MH. Что обычно и применяется в ряде нынешних более-менее продвинутых ЗУ и ЗРУ. В старинной МС3000 это тоже есть, но я всю эту красоту временно отключил, что бы подготовить данный материал.
А при решении реальных задач лучше перестраховаться, ибо ∆V может быть не поймана ввиду недостаточной силы тока или неудачного стечения обстоятельств.
Всего наилучшего. Может, кому-то было интересно.
Несмотря на местами вполне обоснованную критику со стороны продвинутых пользователей разномастного «лития» в мире до сих пор используется огромное количество устройств на Ni-MH «тяге». Скорее всего, речь идет о сотнях миллионов или нескольких миллиардах (ИМХО). От мультиметров, тонометров и мышек до елочных гирлянд, электрических игрушек и прочей бытовухи.
Так что, пока с этим самым морально устаревшим Ni-MH надо как-то жить и как-то бороться с главной проблемой никель-металлгидрида — отсутствием вменяемого алгоритма заряда оного.
Как гарантированно зарядить Ni-MH от 0 до 100% и полностью исключить вредное явление перезаряда? Строго говоря — почти никак. Но заметно сгладить негативные моменты сего действа в принципе возможно при комплексном подходе с применением дополнительных алгоритмов определения момента окончания заряда.
Под катом — экскурс в электрохимию Ni-MH и наглядная демонстрация практического применения «самого продвинутого» метода "-dv/dt" или «минус дельта». Великих открытий там нет, но может кого-то заинтересуют некоторые моменты.
1. Что происходит в ходе заряда Ni-MH?
[Если содержание данного раздела вдруг стало совсем непонятно, то придется все это дело пропустить. Мало чего потеряете, только полная ясность понимания некоторых моментов во 2 разделе не так что бы гарантирована.]
Рассмотрим основные электрохимические (ЭХ) процессы, протекающие при заряде Ni-MH ячейки. Таких процессов три:
☀ Основной заряд (Ni⁺²→Ni⁺³)&(М → МН), т.н. фарадеевский процесс
☀☀ Кислородный цикл
☀☀☀ Переразряд на никелевом электроде Ni⁺³ → Ni⁺⁴
При заряде от 0 до 100% эти процессы протекают всегда и они протекают параллельно. Это конкурирующие реакции. При этом они забирают некоторую долю эл. энергии, подводимой извне. Если добавить неизбежное тепловое рассеяние по Джоулю-Ленцу и не учитывать маловероятные побочные процессы, то получаем полный энергетический баланс:
E(от внешнего источника)=E(основной процесс)+E(кислородный и цикл)+E(Ni⁺³→Ni⁺⁴)+E(джоулево тепло).
Но интенсивности протекания на разных этапах заряда три химических процесса часто сильно отличаются. Поэтому в ряде случаев наличием того или иного процесса можно пренебречь (скорость → 0).
► Так, на начальной стадии заряда до 70-80% DoC***, основной (фарадеевский) процесс (Ni⁺²→Ni⁺³)&(М → МН) является фактически единственным химическим процессом в системе. При этом вся подводимая энергия расходуется на протекание основного процесса и диссипацию в виде джоулева тепла.
 ***Примечание. DoC (Depth of Charge) переводится как «глубина заряда» ячейки или аккумуляторной батареи. Определяется как отношение количества израсходованного электричества при заряде к заявленной (или реальной) емкости. К истинной глубине заряда аккумулятора имеет весьма опосредованное отношение, т.к. часть эл. энергии неизбежно тратится впустую.
***Примечание. DoC (Depth of Charge) переводится как «глубина заряда» ячейки или аккумуляторной батареи. Определяется как отношение количества израсходованного электричества при заряде к заявленной (или реальной) емкости. К истинной глубине заряда аккумулятора имеет весьма опосредованное отношение, т.к. часть эл. энергии неизбежно тратится впустую.Поэтому существует принципиальная возможность сверхбыстрого заряда батарей Ni-MH токами 5-10С до половины или 2/3 емкости. При наличии эффективной системы охлаждения и термоконтроля каждой ячейке в сборке. Но о практической реализации таких проектов я не слышал. В отличии от промышленных батарей Ni-Cd.
► В интервале DoC (Depth of Charge) 70-100% происходит смена преобладающего процесса, потребляющего подводимую энергию с основного (фарадеевского) на кислородный цикл. Кислородный цикл экзотермичен.
►После 95-100%, особенно при больших плотностях тока становится заметным и переразряд (Ni⁺³ → Ni⁺⁴), так же как кислородный цикл идущий с выделением тепла. Потому что переразряд — это тоже цикл (Ni⁺³ ⇆ Ni⁺⁴), но с более медленной диссипацией энергии.
Какие же факторы оказывают влияние на интенсивность протекания трех конкурирующих процессов?
• Уровень заряда ячейки
• Сила тока, протекающего через ячейку
• Температура и давление О₂ в системе
Насчет силы тока — тут есть некоторое лукавство. Ибо сила тока, протекающего через ячейку зависит от величины напряжения, приложенного к ячейке. И именно эта величина оказывает непосредственное влияние на интенсивность протекания ЭХ процессов. Но ЗУ (зарядное устройство) задает именно значение силы тока, а автоматика подбирает нужную разность потенциалов на электродах. Поэтому логичнее оперировать параметром «сила тока».
Рассмотрим эти три процесса подробнее. Внимание - электрохимия!
☀Процесс заряда ячейки (Ni⁺²→Ni⁺³)&(М → МН)
В ходе заряда внутри Ni-MH аккумулятора происходит «перекачка» атомов водорода от ОНЭ (оксидно-никелевый электрод) к МГЭ (MH-электрод).
В ходе разряда процессы протекают в обратном направлении.
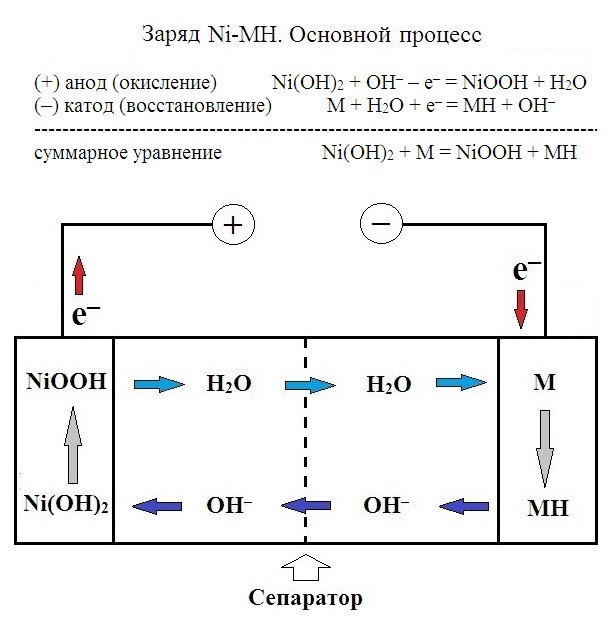 Примечание. На картинке катод и анод определены с т.з. химии (электрохимии). Катод — электрод, на котором протекают процессы восстановления. Анод — электрод, на котором протекают процессы окисления. Если не заряжать, а разряжать ячейку, то катод и анод поменяются местами. Это вносит большую путаницу.
Примечание. На картинке катод и анод определены с т.з. химии (электрохимии). Катод — электрод, на котором протекают процессы восстановления. Анод — электрод, на котором протекают процессы окисления. Если не заряжать, а разряжать ячейку, то катод и анод поменяются местами. Это вносит большую путаницу.
В этой схеме буквой «M» обозначен сплав металлов, очень хорошо растворяющий атомы водорода. То есть, водород с ними образует твердые растворы внедрения, которые тут имеют условное обозначение «МН». В нулевом приближении «М» — это интерметаллид типа LaNi₅, где лантан — металл, растворяющий водород, а никель — «матрица-носитель» и вроде как катализатор (но это не точно).
На самом деле, с составом все несколько сложнее. Вместо чистого лантана экономически выгоднее использовать смесь из 4-х лантаноидов (50-60% La + 30-40% Ce + 10-15% Nd + 1-2% Pr), которая имеет техническое название «мишметалл, обогащенный лантаном».
☀☀ Кислородный цикл
В химических источниках тока с ОНЭ всегда используются электролит, состоящий из воды и гидроксидов щелочных металлов (KOH, NaOH, LiOH), как по отдельности, так и сложных смесях. Вода и гидроксид-ионы ОН⁻ щелочей принимают активное участие в переносе атомов водорода между катодом и анодом как при заряде, так и при разряде ячейки. Кроме того, гидроксид-ионы обеспечивают перенос заряда во внутренней цепи гальванического элемента.
Но наличие воды в системе создает и основные проблемы при эксплуатации ХИТ.
Именно водой обусловлено протекание самого известного побочного процесса, имеющего место в ходе заряда любого аккумулятора с электролитом на водной основе. Это так называемый кислородный цикл.
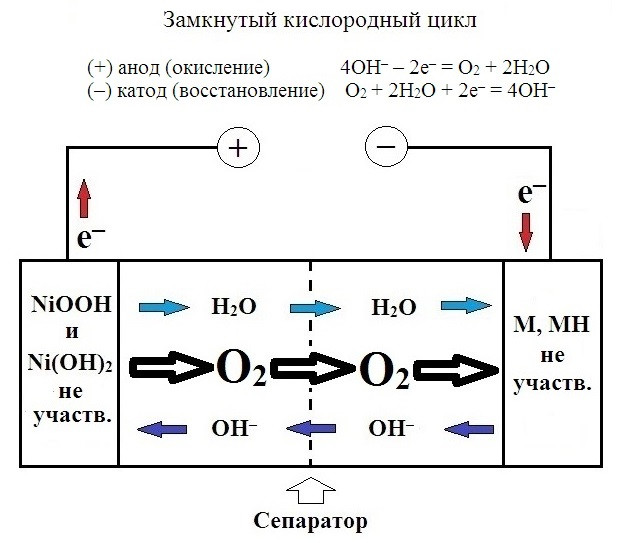 Кислородный цикл присутствует на протяжении всего процесса заряда аккумулятора, но становится хоть как-то заметным при наборе 60-70% зарядной емкости ячейки. После ~80% кислородный цикл по интенсивности становится сравним с основным процессом заряда, представленным выше. А после 100% – главным и почти единственным в системе. Но чем больше ток заряда, тем большую конкуренцию кислородному циклу составляет процесс Ni⁺³ → Ni⁺⁴ (см. ниже).
Кислородный цикл присутствует на протяжении всего процесса заряда аккумулятора, но становится хоть как-то заметным при наборе 60-70% зарядной емкости ячейки. После ~80% кислородный цикл по интенсивности становится сравним с основным процессом заряда, представленным выше. А после 100% – главным и почти единственным в системе. Но чем больше ток заряда, тем большую конкуренцию кислородному циклу составляет процесс Ni⁺³ → Ni⁺⁴ (см. ниже).
Кислородный цикл — это побочный процесс, причем экзотермический (идет с выделением теплоты). Не только бесполезный, но и вредный. Электроэнергия тратится впустую, превращается в тепло, а значит увеличивается температура. Обратите внимание — это не джоулево тепло. Это как бы «химическая» добавка к джоулеву теплу: суммарная теплота, выделяющаяся при протекании двух химических процессов — генерации молекул О₂ на МГЭ и их уничтожении на ОНЭ. На картинке ниже кривульки, снятые для процесса заряда 4 ячеек АА током 0.5С (1.1А):
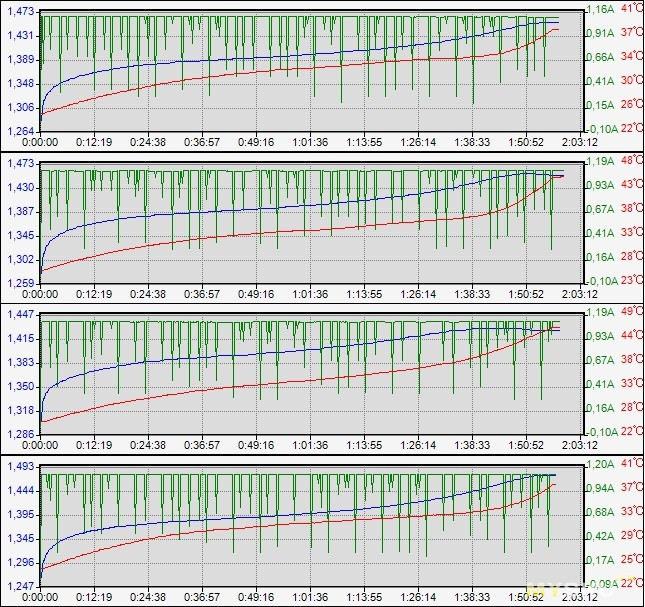 Такие графики выдает программа MC3000_Monitor.
Такие графики выдает программа MC3000_Monitor.
Красные кривые — температура. Хорошо заметный резкий подъем Т на заключительной стадии заряда — за счет активного протекания кислородного цикла. Следует понимать, что ячейки отличаются по емкости и находятся на немного разных стадиях завершения заряда. Для обр. №1 и №4 экстремум напряжения еще не достигнут. А для обр. №2 и №3 — уже пройден, через несколько минут произойдет остановка процесса после выполнения условия ∆V = — 3 mV. Соответственно, и температуры обр. №2 и №3 выше на несколько градусов.
За счет протекания кислородного цикла в герметичной банке растет давление. Не столько от нагревания, сколько от недостаточной эффективности процесса «уничтожения» газообразного кислорода на катоде.
Производители всячески борются с этим нехорошим явлением: в активную массу ОНЭ добавляют кобальт (раньше – барий), в электролит (обычно КОН) – гидроксид лития LiOH. Все эти добавки повышают перенапряжение выделения газообразного кислорода — тем самым уменьшают интенсивность его выделения, увеличивают эффективность и безопасность процесса заряда. Но полностью подавить выделение кислорода на аноде не удается. И не удастся никогда.
Некоторые думают, что кислородный цикл и есть тот самый перезаряд аккумулятора, коего следует боятся больше всего. Ан нет.
☀☀☀ Переразряд на никелевом электроде Ni⁺³ → Ni⁺⁴
К перезаряду приводит другой процесс. Он изображен на рисунке.
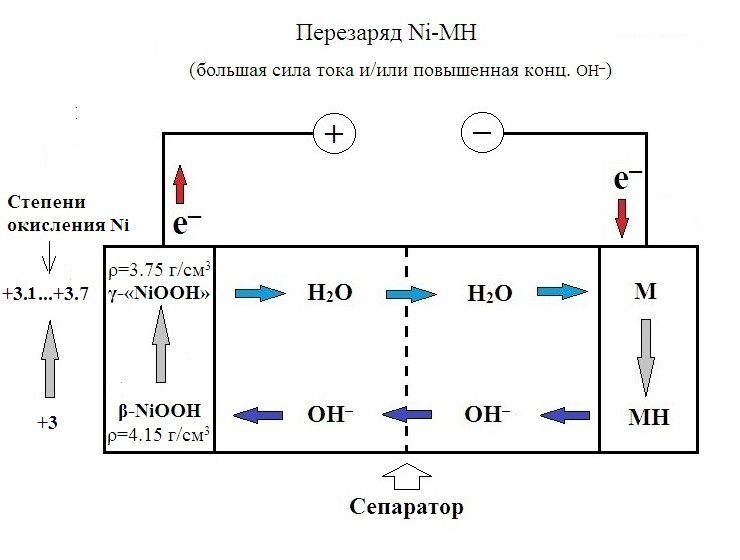 О чем эта картинка? Напомню, что с точки зрения химии, в ходе заряда активная масса ОНЭ окисляется. Конкретнее – происходит дегидрогенизация (потеря водорода) гидроксида никеля (+2) по схеме: β-Ni(OH)₂ – Н → β-NiOOH. Об этом было уже рассказано выше. В гидроксиде никеля степень окисления +2, а в β-NiOOH она равна +3. То есть, в процессе заряда (окисления) ОНЭ средняя температура по больнице (зачеркнуто) усредненная степень окисления никеля плавно повышается от +2 до +3.
О чем эта картинка? Напомню, что с точки зрения химии, в ходе заряда активная масса ОНЭ окисляется. Конкретнее – происходит дегидрогенизация (потеря водорода) гидроксида никеля (+2) по схеме: β-Ni(OH)₂ – Н → β-NiOOH. Об этом было уже рассказано выше. В гидроксиде никеля степень окисления +2, а в β-NiOOH она равна +3. То есть, в процессе заряда (окисления) ОНЭ средняя температура по больнице (зачеркнуто) усредненная степень окисления никеля плавно повышается от +2 до +3.
После того как Ni(OH)₂ полностью превратился в β-NiOOH оксидно-никелевый электрод считается (и является) полностью заряженным. Но если продолжать процесс «заряда» ячейки, то начинает протекать процесс: β-NiOOH ---> γ-NiOOH. Что такое «γ-NiOOH»? Это фаза переменного состава NiOх(OH)y, где x>1 и y<1. Другими словами, это β-NiOOH, потерявший часть водорода. Если уж совсем по-простому, то это как бы смесь β-NiOOH и высшего оксида никеля NiO₂. Не трудно определить степень окисления никеля в NiO₂. Она равна +4.
Оксид никеля (+4) – вещество крайне неустойчивое и начинает разлагаться с выделением газообразного кислорода уже в процессе получения. Кстати, чем выше температура, тем шустрее разлагается NiO₂, а выделяющийся кислород «уничтожается» на отрицательном электроде с большей скоростью. А вот само наличие в системе газообразного кислорода, да под высоким давлением («спасибо» кислородному циклу) препятствует разложению NiO₂, а значит способствует его накоплению в активной массе ОНЭ. Величина силы тока тоже влияет на это. Чем она больше, тем быстрее идет «генерация» оксида никеля (+4), а значит выше его «концентрация» в γ-NiOOH. А значит, бОльший объем γ-NiOOH вовлекается в этот процесс.
Это и есть так называемый «перезаряд». Бессмысленный и вредный процесс получения-разложения избыточно окисленной кислородсодержащей фазы никеля.
В ходе заряда внутри Ni-MH аккумулятора происходит «перекачка» атомов водорода от ОНЭ (оксидно-никелевый электрод) к МГЭ (MH-электрод).
В ходе разряда процессы протекают в обратном направлении.
 Примечание. На картинке катод и анод определены с т.з. химии (электрохимии). Катод — электрод, на котором протекают процессы восстановления. Анод — электрод, на котором протекают процессы окисления. Если не заряжать, а разряжать ячейку, то катод и анод поменяются местами. Это вносит большую путаницу.
Примечание. На картинке катод и анод определены с т.з. химии (электрохимии). Катод — электрод, на котором протекают процессы восстановления. Анод — электрод, на котором протекают процессы окисления. Если не заряжать, а разряжать ячейку, то катод и анод поменяются местами. Это вносит большую путаницу.В этой схеме буквой «M» обозначен сплав металлов, очень хорошо растворяющий атомы водорода. То есть, водород с ними образует твердые растворы внедрения, которые тут имеют условное обозначение «МН». В нулевом приближении «М» — это интерметаллид типа LaNi₅, где лантан — металл, растворяющий водород, а никель — «матрица-носитель» и вроде как катализатор (но это не точно).
На самом деле, с составом все несколько сложнее. Вместо чистого лантана экономически выгоднее использовать смесь из 4-х лантаноидов (50-60% La + 30-40% Ce + 10-15% Nd + 1-2% Pr), которая имеет техническое название «мишметалл, обогащенный лантаном».
☀☀ Кислородный цикл
В химических источниках тока с ОНЭ всегда используются электролит, состоящий из воды и гидроксидов щелочных металлов (KOH, NaOH, LiOH), как по отдельности, так и сложных смесях. Вода и гидроксид-ионы ОН⁻ щелочей принимают активное участие в переносе атомов водорода между катодом и анодом как при заряде, так и при разряде ячейки. Кроме того, гидроксид-ионы обеспечивают перенос заряда во внутренней цепи гальванического элемента.
Но наличие воды в системе создает и основные проблемы при эксплуатации ХИТ.
Именно водой обусловлено протекание самого известного побочного процесса, имеющего место в ходе заряда любого аккумулятора с электролитом на водной основе. Это так называемый кислородный цикл.
 Кислородный цикл присутствует на протяжении всего процесса заряда аккумулятора, но становится хоть как-то заметным при наборе 60-70% зарядной емкости ячейки. После ~80% кислородный цикл по интенсивности становится сравним с основным процессом заряда, представленным выше. А после 100% – главным и почти единственным в системе. Но чем больше ток заряда, тем большую конкуренцию кислородному циклу составляет процесс Ni⁺³ → Ni⁺⁴ (см. ниже).
Кислородный цикл присутствует на протяжении всего процесса заряда аккумулятора, но становится хоть как-то заметным при наборе 60-70% зарядной емкости ячейки. После ~80% кислородный цикл по интенсивности становится сравним с основным процессом заряда, представленным выше. А после 100% – главным и почти единственным в системе. Но чем больше ток заряда, тем большую конкуренцию кислородному циклу составляет процесс Ni⁺³ → Ni⁺⁴ (см. ниже). Кислородный цикл — это побочный процесс, причем экзотермический (идет с выделением теплоты). Не только бесполезный, но и вредный. Электроэнергия тратится впустую, превращается в тепло, а значит увеличивается температура. Обратите внимание — это не джоулево тепло. Это как бы «химическая» добавка к джоулеву теплу: суммарная теплота, выделяющаяся при протекании двух химических процессов — генерации молекул О₂ на МГЭ и их уничтожении на ОНЭ. На картинке ниже кривульки, снятые для процесса заряда 4 ячеек АА током 0.5С (1.1А):
 Такие графики выдает программа MC3000_Monitor.
Такие графики выдает программа MC3000_Monitor.Красные кривые — температура. Хорошо заметный резкий подъем Т на заключительной стадии заряда — за счет активного протекания кислородного цикла. Следует понимать, что ячейки отличаются по емкости и находятся на немного разных стадиях завершения заряда. Для обр. №1 и №4 экстремум напряжения еще не достигнут. А для обр. №2 и №3 — уже пройден, через несколько минут произойдет остановка процесса после выполнения условия ∆V = — 3 mV. Соответственно, и температуры обр. №2 и №3 выше на несколько градусов.
За счет протекания кислородного цикла в герметичной банке растет давление. Не столько от нагревания, сколько от недостаточной эффективности процесса «уничтожения» газообразного кислорода на катоде.
Производители всячески борются с этим нехорошим явлением: в активную массу ОНЭ добавляют кобальт (раньше – барий), в электролит (обычно КОН) – гидроксид лития LiOH. Все эти добавки повышают перенапряжение выделения газообразного кислорода — тем самым уменьшают интенсивность его выделения, увеличивают эффективность и безопасность процесса заряда. Но полностью подавить выделение кислорода на аноде не удается. И не удастся никогда.
Некоторые думают, что кислородный цикл и есть тот самый перезаряд аккумулятора, коего следует боятся больше всего. Ан нет.
☀☀☀ Переразряд на никелевом электроде Ni⁺³ → Ni⁺⁴
К перезаряду приводит другой процесс. Он изображен на рисунке.
 О чем эта картинка? Напомню, что с точки зрения химии, в ходе заряда активная масса ОНЭ окисляется. Конкретнее – происходит дегидрогенизация (потеря водорода) гидроксида никеля (+2) по схеме: β-Ni(OH)₂ – Н → β-NiOOH. Об этом было уже рассказано выше. В гидроксиде никеля степень окисления +2, а в β-NiOOH она равна +3. То есть, в процессе заряда (окисления) ОНЭ средняя температура по больнице (зачеркнуто) усредненная степень окисления никеля плавно повышается от +2 до +3.
О чем эта картинка? Напомню, что с точки зрения химии, в ходе заряда активная масса ОНЭ окисляется. Конкретнее – происходит дегидрогенизация (потеря водорода) гидроксида никеля (+2) по схеме: β-Ni(OH)₂ – Н → β-NiOOH. Об этом было уже рассказано выше. В гидроксиде никеля степень окисления +2, а в β-NiOOH она равна +3. То есть, в процессе заряда (окисления) ОНЭ средняя температура по больнице (зачеркнуто) усредненная степень окисления никеля плавно повышается от +2 до +3.После того как Ni(OH)₂ полностью превратился в β-NiOOH оксидно-никелевый электрод считается (и является) полностью заряженным. Но если продолжать процесс «заряда» ячейки, то начинает протекать процесс: β-NiOOH ---> γ-NiOOH. Что такое «γ-NiOOH»? Это фаза переменного состава NiOх(OH)y, где x>1 и y<1. Другими словами, это β-NiOOH, потерявший часть водорода. Если уж совсем по-простому, то это как бы смесь β-NiOOH и высшего оксида никеля NiO₂. Не трудно определить степень окисления никеля в NiO₂. Она равна +4.
Оксид никеля (+4) – вещество крайне неустойчивое и начинает разлагаться с выделением газообразного кислорода уже в процессе получения. Кстати, чем выше температура, тем шустрее разлагается NiO₂, а выделяющийся кислород «уничтожается» на отрицательном электроде с большей скоростью. А вот само наличие в системе газообразного кислорода, да под высоким давлением («спасибо» кислородному циклу) препятствует разложению NiO₂, а значит способствует его накоплению в активной массе ОНЭ. Величина силы тока тоже влияет на это. Чем она больше, тем быстрее идет «генерация» оксида никеля (+4), а значит выше его «концентрация» в γ-NiOOH. А значит, бОльший объем γ-NiOOH вовлекается в этот процесс.
Это и есть так называемый «перезаряд». Бессмысленный и вредный процесс получения-разложения избыточно окисленной кислородсодержащей фазы никеля.
2. Режимы заряда и способы определения момента окончания заряда (отсечка)
[В качестве исходника для данного раздела взята статья известного фонаревщика датчанина HKJ и заметно переработана: опущено малосущественное, добавлено недостающее (ИМХО).]
Надежного критерия окончания заряда не существует. Поэтому таких способов напридумано множество. И в интернетах говорено о них много раз. Одно плохо — практически все знают что происходит с напряжением и температурой в процессе заряда, но не понимают почему это происходит. Ибо химический источник тока для человека, не замутненного электрохимией, по сути «черный ящик» или «вещь в себе» (Кант).
Но мы, вооружившись материалом из разд.1, попробуем разобраться.
Особое внимание будет уделено методу "-∆V", а про все остальные — вскользь.
Зарядка малым током (Low current charging)
Про «древний» и «сверхмедленный» заряд «никелевых» ячеек (Ni-Cd и Ni-MH) многие слышали. Заряд током 0.1С, отсечка по времени через 14-16 часов.
Но самое интересное, что этот способ заряда самый надежный и наименее вредный для потрохов аккумулятора. Перезаряд (в химическом понимании) там присутствует, но он ничтожно мал. Почему? Идея проста: за первые 7-8 часов элемент набирает 70-80% номинальной емкости. Потом начинает заметно протекать кислородный цикл, который чем дальше, тем больше пожирает подводимое электричество. Тем не менее, элемент за оставшиеся 6-8 час. неспешно добирает оставшуюся емкость до фактической максимальной. Ввиду малости зарядного тока переразряд на никелевом электроде (Ni⁺³ → Ni⁺⁴) стремится к нулю и его можно не учитывать.
Теперь становиться понятным почему в рекомендациях МЭК (калька с английского — ГОСТы) на протяжении многих лет присутствует один интересный момент
ссылка
 В подавляющем большинстве современных ЗУ Low current charging отсутствует, он там не нужен. В SkyRC MC3000 — есть. Исключительно для проверки по ГОСТу.
В подавляющем большинстве современных ЗУ Low current charging отсутствует, он там не нужен. В SkyRC MC3000 — есть. Исключительно для проверки по ГОСТу.Отсечка по напряжению (Voltage termination)
Метод прост как трусы. При постоянном токе заряжаем до момента, пока напряжение не достигнет определенного значения.
Используется во многих недорогих ЗУ. Самый известный пример — Lii-500. ТУТ обзор от датчанина HKJ.
 Рекомендуется замерять разность потенциалов на электродах при кратковременном снятии нагрузки, т.е. НРЦ (напряжение разорванной цепи). Так получается точнее.
Рекомендуется замерять разность потенциалов на электродах при кратковременном снятии нагрузки, т.е. НРЦ (напряжение разорванной цепи). Так получается точнее.Проблемой данного метода является то, что измеренное значение НРЦ зависит от температуры и скорости заряда (поляризация электродов, которая не может рассосаться мгновенно), что создает дополнительные головняки.
 Триггерное значение НРЦ производителями ЗУ подбирается в предположении температуры 20-30°С. Если заряд производится в шибко холодном помещении и на малых токах, то весьма вероятен заметный недозаряд. Но еще хуже, если все это происходит на жаре и при больших токах без принудительного охлаждения — возможно не выполнение условия остановки процесса и «бесконечный» заряд.
Триггерное значение НРЦ производителями ЗУ подбирается в предположении температуры 20-30°С. Если заряд производится в шибко холодном помещении и на малых токах, то весьма вероятен заметный недозаряд. Но еще хуже, если все это происходит на жаре и при больших токах без принудительного охлаждения — возможно не выполнение условия остановки процесса и «бесконечный» заряд.Отсечка по "-∆V" (-dv/dt termination)
Нынешние продвинутые ЗУ часто определяют момент окончания заряда Ni-MH/Ni-Cd по критерию "- ∆V". Кратковременное снижение разности потенциалов между электродами ячейки (- ∆V) происходит где-то вблизи окончания заполнения ячейки. Но какова природа наблюдаемого — ∆V?
Предположительно, происходит следующее.
1) Как уже было отмечено, чем ближе ячейка к состоянию полного заряда, тем более вяло протекает основной процесс (Ni⁺²→Ni⁺³)&(М → МН) и сильнее выражен кислородный цикл. Активное протекание кислородного цикла приводит к тому, что бОльшая часть подводимой эл. энергии превращается в тепло. Если бы не перезаряд Ni⁺³ → Ni⁺⁴, то при уровне заряда ячейки 100% в тепло превращалась бы вся энергия (кислородный цикл + джоулево тепло).
2) Итак, при приближении ячейки к состоянию полного заряда наблюдается резкий рост Т. Что приводит к увеличению проводимости электролита (р-р КОН)
 3) Для того, что бы ток, протекающий через ячейку, оставался постоянным (равным заданному) ЗРУ автоматически начинает снижать внешнюю разность потенциалов. В результате получаем горб на кривой напряжения. Правый склон того горба — это и есть «эффект -∆V» или "«минус дельты».
3) Для того, что бы ток, протекающий через ячейку, оставался постоянным (равным заданному) ЗРУ автоматически начинает снижать внешнюю разность потенциалов. В результате получаем горб на кривой напряжения. Правый склон того горба — это и есть «эффект -∆V» или "«минус дельты».
 4) И опять-таки рекомендуется замерять разность потенциалов на электродах при кратковременном снятии нагрузки, т.е. НРЦ (напряжение разорванной цепи).
4) И опять-таки рекомендуется замерять разность потенциалов на электродах при кратковременном снятии нагрузки, т.е. НРЦ (напряжение разорванной цепи).  5) Чтобы достаточно надежно поймать "- ∆V" датчанин рекомендует использовать токи не ниже 0.5С. Но, как было отмечено выше, бОльшие токи заряда способствуют переокислению β-NiOOH до γ-NiOOH (или NiO₂) и ускорению деградации активной массы «никелевого» электрода.
5) Чтобы достаточно надежно поймать "- ∆V" датчанин рекомендует использовать токи не ниже 0.5С. Но, как было отмечено выше, бОльшие токи заряда способствуют переокислению β-NiOOH до γ-NiOOH (или NiO₂) и ускорению деградации активной массы «никелевого» электрода.Прерывание 0dv/dt (0dv/dt termination)
При малых токах зарядки эффект "- ∆V" исчезает. Вместо того чтобы искать падение напряжения, можно искать стабильное напряжение (или даже очень медленно растущее напряжение) и использовать его в качестве критерия окончания зарядки.
Метод несколько стремен в реализации и обычно используется как дополнение к "- ∆V", ежели та самая «дельта» по каким-то причинам не была «поймана».

~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~
3. Опыты
Для опытов было выбрано четыре БУ-шных аккумулятора ААА:
EN-1 и EN-2
Panasonic Eneloop BK-4MCCE даташит
FU-1 и FU-2
Fujitsu HR-4UTC даташит (дубль)
Все они сделаны на заводе Fujitsu (FDK) по одной и той же технологии и отличаются только наклейками.
 Поэтому и [краткие] даташиты у них фактически одинаковы.
Поэтому и [краткие] даташиты у них фактически одинаковы.Давайте разберемся что там понаписано и нарисовано.
 Т.н. «ёмкость» акку заявлена в двух вариантах:
Т.н. «ёмкость» акку заявлена в двух вариантах:— минимальная (750 мАч)
— типичная (800 мАч)
Прикол в следующем — до 2011 г. производители (или вендоры) аккумуляторов могли заявлять для них ёмкость «как они ее видят» и указывать оную прямо на наклейке.
Но в IEC 61951-2:2011 МЭК обязал дополнительно указывать на наклейке минимально гарантированную ёмкость, хотя бы мелким шрифтом.
 На картинках заряда и разряда показано, что заряд ячеек производится током 800мА, а критерием завершения заряда является ∆V=-10мВ. Вот от этого и будем далее танцевать.
На картинках заряда и разряда показано, что заряд ячеек производится током 800мА, а критерием завершения заряда является ∆V=-10мВ. Вот от этого и будем далее танцевать.В опытах использовалась известное ЗРУ SkyRC MC3000. Для Ni-MH оно позволяет выставить значение ∆V от -3 до -20мВ. Замеры на предмет поимки ∆V производятся при кратковременном отключении нагрузки 3 раза в минуту.
Так же использовалась «родная» утилита MC3000_Monitor_V1.06, которая:
• [главное] записывает лог с интервалом 1 сек. в файл *.CSV
• [дополнительно] отображает что происходит в графическом окне
Графическая часть весьма примитивна и практически не настраивается. Имеет глюк с отображением оси времени (занижает на 3-4 мин. в течении каждого часа). Но смысл оной — дать только общее представление о происходящем.
Предварительно было проверена адекватность образцов.
5 циклов заряд (0.5А, ∆V=-3мВ) → пауза(30мин) → разряд (0.5А) → пауза (30мин).
Если нужно, нарисую табличку. Все равно, измеренные значения емкости не являются «гостовскими»: режимы заряда и разряда «неправильные» и паузы меньше часа:).
Опыты проводились единообразно: один цикл заряд-разряд.
Заряд (I(заряда), ∆V) → пауза(60мин) → разряд (0.16А до 1.00В)
I(заряда)=800...300мА
∆V=-10 или -3мВ
Опыт №1. I(заряда)=800мА, ∆V=-10мВ
Все прошло нормально, ∆V=-10мВ зафиксирована для всех 4 образцов. Интересно, что максимум температуры всегда наблюдается чуть позже момента остановки заряда.
 Чуть подробнее на основании лога (в качесте примера — EN-1)
Чуть подробнее на основании лога (в качесте примера — EN-1)
 Краткая сводка:
Краткая сводка:
Опыт №2. I(заряда)=500мА, ∆V=-10мВ
И опять ∆V=-10мВ зафиксирована для всех 4 образцов.
 Краткая сводка:
Краткая сводка:
Опыт №3. I(заряда)=300мА, ∆V=-10мВ
«Дельта» НЕ зафиксирована для всех 4 образцов. Хотя ждал чуть более 4 часов. На графиках время занижено, это глюк граф. интерфейса утилиты (см. выше)
 Краткая сводка:
Краткая сводка: Причина вполне очевидна: для всех образцов реальное значение ∆V не дотянуло до -10мВ…
Причина вполне очевидна: для всех образцов реальное значение ∆V не дотянуло до -10мВ…
 Здесь есть один нюанс: в лог записываются «верхние» значения напряжения, а определение ∆V происходит по «нижним», в моменты пауз, которые в лог не пишутся. Но ∆V по «нижним» или такая же как по «верхним» или чуть меньше.
Здесь есть один нюанс: в лог записываются «верхние» значения напряжения, а определение ∆V происходит по «нижним», в моменты пауз, которые в лог не пишутся. Но ∆V по «нижним» или такая же как по «верхним» или чуть меньше.Что же делать в такой ситуации? Есть 2 варианта решения возникшей проблемы:
• или увеличить I(заряда)
• или уменьшить ∆V (по модулю)
Собственно, два заключительных опыта будут этому и посвящены.
Посмотрим, что получится.;)
Опыт №4. I(заряда)=300 → 400мА, ∆V=-10мВ
Увы, «дельта» была «поймана» только для 2 образцов Фуджи.
 Энелупы таки «слили», но были близки к выполнению условия по ∆V:
Энелупы таки «слили», но были близки к выполнению условия по ∆V: Формально, для EN-1 условие ∆V=-10 на 20 сек. было выполнено.
Формально, для EN-1 условие ∆V=-10 на 20 сек. было выполнено. Но это для «верхних» значений напряжения (под нагрузкой). А вот для «нижних» (без нагрузки), скорее всего, нет. А именно по вторым и ловится та самая «дельта».
Но это для «верхних» значений напряжения (под нагрузкой). А вот для «нижних» (без нагрузки), скорее всего, нет. А именно по вторым и ловится та самая «дельта».У Фуджей все хорошо:

Но в результатах опыта №4 есть пока необъяснимая странность.
Посмотрите на сводную табличку и сравните чиселки, полученные для EN-2 и FU-2
 Для EN-1
Для EN-1 — меньше измеренная (текущая) емкость
— больше пиковая температура при заряде
Если я правильно понимаю, оба этих момента благоприятствуют тому, что успешная поимки «дельты» более вероятна для EN-2, а не для FU-2.
Но произошло все с точностью до наборот.
Чертовщина какая-то.
Опыт №5. I(заряда)=300мА, ∆V=-10 → -3мВ
И опять «дельта» была «поймана» только для 2 образцов Фуджи....

Энелупы опять «слили». Наверное, какая-то черная полоса:

А с Фуджи по-прежнему все нормально:

Влияние силы тока заряда на величины измеренных емкостей
Ну и в конце — влияние I(заряда) на величины измеренных емкостей (энергоемкостей) при фиксированном значении ∆V=-10мВ. Тенденция вроде как прослеживается, но не так что бы фатальная:
 Причем, для EN-1 и EN-2 при 300 и 400 мА «дельта» не была поймана. Поэтому измеренные значения «ёмкости» для 300 и 400 мА:
Причем, для EN-1 и EN-2 при 300 и 400 мА «дельта» не была поймана. Поэтому измеренные значения «ёмкости» для 300 и 400 мА:— фактически одинаковы;
— вполне возможно, что несколько завышены.
Заключение
Вот такой он, метод "-∆V". «Самый продвинутый» и при этом самый капризный из всех ныне используемых. Ибо должно выполнится ряд условий и ЗУ в течении отлавливания «дельты» (а это не одна минута) не должно учудить вверх ни на милливольт по НРЦ во время краткосрочных пауз по нагрузке.
И что делать? Использовать
А при решении реальных задач лучше перестраховаться, ибо ∆V может быть не поймана ввиду недостаточной силы тока или неудачного стечения обстоятельств.
Всего наилучшего. Может, кому-то было интересно.
Самые обсуждаемые обзоры
| +125 |
4227
163
|
| +69 |
2935
56
|
| +69 |
3365
56
|
(вентилятор\внешнее перепад=сквозняк) температура должна подняться минимум на 15 градусов
p/s
а так весь это никель в эпоху лития (АА\ААА\кроны) уже только для энтузиастов \староверов
P.S. Не, я не к тому, что литий не нужен, я к тому, что пока Ni-MH аккумы у меня есть, я не буду принудительно менять их на литий только из-за того, что он быстрее заряжается. Вот умрут, тогда и буду думать.
Давно экспериментировал и сделал для себя вывод — ток устанавливаем минимум 0,25А (на разрядку) и 0,5А на зарядку. Выкидываем весь мусор из дома и покупаем брендовые аккумуляторы.
Всё, проблема закрывается и про ∆V больше не вспоминаешь и никто не делает нервы. По крайней мере на своём старом аппарате TechnoLine BC-700 (La Crosse).
Аккумуляторы Panasonic Eneloop живут в таком режиме много лет — белые и чёрные.
Когда вдруг надо срочно, а аккумы разряжены — вдуваю от лабораторника 5 ампер в течение 15 минут.
Хрен его знает, что с этими лакроссами происходит, ну да, кнопки там эээ… но у меня контачат нормально, проверял. Кондеры тоже менял. Всё равно галюнит, был брошен в коробку с электронным хламом.
проще махой. но она cv/cc, хотя при более-менее стабильной комнатной температуре это не проблема. и кнопки для запуска жать надо.
а еще проще hg1412. тоже самое, но нет предварительного контроля внутреннего сопротивления.
И таки да, аккумы в этой зарядке так люто не греются, справедливости ради следует отметить что она в своей быстрой фазе все же их немного не дозаряжает, но тем не менее если нет спешки, то она добъет их до 100%
Спасибо за труд, всегда интересно почитать со школьным уровнем знания химии.
За многие годы только однажды LiFePo оригиналы от отцов основателей- фирмы A123, были возвращены к состоянию новых после разряда до 0.1В. сравнивал графики разряда в одинаковых условиях.
Иногда при полной разрядке удается ЛБП оживить Li-ION 18650. Чаще не удается.
А оживление Li-Ion плохая затея. Нашёл фонарь из фикс-прайса, который не проверяет на глубокий разряд. Сначала использовал провод, который давал максимум 0.33А зарядный ток, потом нашёл который давал 0.9А. Потом с али долго ждал микросхему контроллера заряда и светодиод, потом продолжил с током 0.33А. Подтянул до 3.2В, и с помощью Lii-500 зарядил. После чего двое суток ждал, пока аккумулятор разрядится и остынет. Всего таких 8 штук было, которые умерли. Без защиты, темно-коричневые Liitokala, 3000мАч. Оказалось что в устройстве нет защиты от полного разряда.
Плохая идея восстанавливать 18650.
Может эти «блатные» параметры только в дорогих зарядках можно выбирать?
а зачем?всё равно не купить там.лет 15-20 назад были наборчики (зу+акб) «15минутной зарядкой». бренд уже не помню. стоили они как паравоз, так что энтузиазма не вызывали.
p.s. а что вызывает ускоренный разогрев литий-ионных в самом конце разряда (стабильным током)?
mysku.club/blog/russia-stores/105197.html — там есть гнрафик температуры, и на 2.5А, он в конце резко задирается, сходе у обоих видов. на больших это не так заметно, (тем более графики не все получились), но на одном тоже эффект просматривается.
Возможно и обычные литий ионные при заряде до 4.2В начинают слега саморазряд проявлять
а утечка при заряде да, бывает, и что забавно — у меня есть которым сначала поплохело, до 3.9, а потом почти восстановились, в заряднике уже не греются, а за несколько дней где-то до 4.1 опустились и встали.
Ее еще датчанин тестировал.
А Вы счет помните?
3(по дельте):5(по напряжению).
Ну и нафига там «дельта», если ее толком не может поймать?
Но к самой Lii-100 у меня нет претензий. Я ее много раз рекламировал в разных комментах и обзорах. Особенно хорошо было, когда она (или один из десятка ее клонов) на али покупалась за 200-250 рэ… ;)
Мне спокойней когда эта функция присуствует, даже если и не срабатывает.
Я еще застал время когда на гербесте Ли-100 можно было урвать за 1-2 доллара.
Даже боюсь спросить откуда такие умозаключения. «Никель» бывает сильно разный, как и приснопамятный «литий», особенно наиболее часто используемый нонче китайский...:)
Что там еще в доме есть, ну всякие пульты и часы, но они и от копеечных батареек работают больше года, на кой черт в них дорогие аккумуляторы ставить, я не знаю.
Если только игрушки, про них не знаю. Последний раз игрушки покупал 15 лет назад, там уже литий был.
Так где этот
миллионмиллиард nimh аккумуляторов?Весьма наивно отрицать очевидную очевидность. И бежать не только впереди паровоза, но и впереди планеты всей. Это удел наивных хипстеров, но ни как не джельтменов. ИМХА такая.
Так ведь в пользовании юзеров.
Так ведь юзеры утверждают, что это окаменелые экскременты мамонта и у них давно литий везде.
Кроме того рефлектометра, у меня на энелупах еще древний canon sx100 (2007 год). Когда он начинает ругаться на батарею, можно с карты CHDK прогрузить. В принципе, можно в него литий интегрировать, а зачем, за прошлый год я на него примерно 80 кадров кота сделал и всё. Когда энелупы совсем сдохнут, тогда и озадачусь литием, если до той поры какой другой аппарат для фото кота не куплю.
Но попробуйте, если интересно, старые спортивные зарядки. iCharger, Bantam, Schulze, Duratrax. Они уверенно ловят Дельту, если не делать глупостей типа тонких длинных проводов на ветру.
И с чего вдруг такая уверенность, что они более уверенно ловят Дельту, чем МС3000?)
Тайный смысл данной был публикации как раз в том, что даже столь совершенные устройства по ловле дельты (типа МС3000) при определённом стечении обстоятельств могут ее не поймать. А уж про iCharger, Bantam, Schulze, Duratrax… Лучше умолчать. Пожалуйста, не обижайтесь.
Самодельные медное жало для 100Вт пайки встык в уголке до сих пор где-то валяется.
Возможно, мы говорим о разных банках? Наши силовые всегда рядились током 1C, т.е. в районе 3.6-4.2А, и в этом случае дельта ловилась более уверенно, чем .2-.5С, когда да, можно было и не поймать.
Если было достаточно времени, заряжали 0.1С, 16 часов.
Теперь ссылки на тех. описания и даташиты всей ботвы выложите, плиз.
Теперь только LiPo. Максимум найду насадку на паяльник в барахле для пайки встык. Можно ещё нагуглить фотки селекционеров банок, с сотнями банок на столах. Но для меня это дикий кошмар, не буду искать :) с приходом лития это все ушло как страшный сон.
P.S. емнип, даташитах банок которые мы использовали, был критерий либо дельта, либо температура, опять таки емнип, 54градуса. Всегда использовал и дельту, и термодатчик при зарядке. И если дельта прилетала раньше- почти всегда, добавлял ещё капельным, до срабатывания термо. Банки никто не берег, нужна победа здесь и сейчас. На следующие соревнования все равно новые покупать.
На горячих банках и ехали. Ток они отдавали бодрее чем холодные.
но, боюсь, большинству пользователей подход с одноразовыми аккумуляторами не подойдет. ибо цель этой ловли вовсе не в самом спортивном факте, что б он прожил дольше.
Вот выдувалось- да, средний около 30-35А. за 6 минут.
— на токе 0.5С дельта ~5-10 мВ ловится практически всегда
— на токе 0.2С дельта отсутствует
лучшие для него аккумы — литий. и никаких дельт ловить не надо.
Пока пользую Tollkitrc, но уже полгода проектирую и тестирую свою зарядку.
Не знаю, ещё много лет назад было ощущение, что не нужно это разнообразие аккумуляторов и батареек, так что случись, и будем на AA, AAA, C и D сидеть. Да и удобны они форматом — аккумулятор сел, зашёл в магазин, купил батарейки и радуешься. И если каким-то прибором не пользуешься, просто вытаскиваешь аккумуляторы, и ничего не происходит с прибором. Что дальномеры, что фонари, что другая техника. Eneloop не помню с какого года, 8 шт AA, 8 шт AAA. AA покупал в La Crosse, ёмкость как у новых до сих пор. 10 лет им точно есть что одним, что другим.
Самое странное — NiCD в роботе-пылесосе. Тому вообще не помню сколько лет. Вот они-то почему работают? Они обычно дохнут как мухи. Может там какое хитрое зарядное устройство встроено?
Зарядное Varta с микропроцессорным контроллером (аж 2 разных) — сколько аккумуляторов полегло. Уже потом нормальная инструкция попалась, но… тогда уже были другие зарядные устройства. Даже больше не пытался использовать их. Тот же BC-700 сказка. Старые аккумуляторы не оживил, но не дал умереть имеющимся. Сейчас Lii-500 для них и 18650.
Для NiMH зарядный ток 700мА для 1900мАч и 300 для 800мАч. В последнее время без тренировок и полного разряда. Хотя для NiMH рекомендуется после каждых 20 циклов заряда делать с разрядом перед зарядом.
Да, забыл. Там термодатчики. Увы, чаще один на 2 элемента. Сейчас не помню, по-моему только у MAHA на каждый элемент.
И с ними никогда не было проблем с окончанием заряда. Ни со старыми NiMH, ни с NiCD, ни с eneloop.
Я делал кучу попыток обнаружить сей эффект у всяких разных NiMH… и не смог четко зафиксировать. Зато накатал целых 2 статьи по результатам тестов.:)
Сейчас у меня только Fujitsu Eneloop, которые, как известно, не продаются из-за того, что Panasonic купила эту компанию (во всяком случае такое читал). У них да, не наблюдаю эффекта памяти. Но кроме Panasonic Eneloop среди NiMH много другого барахла выпускается. Благодаря статье решил посмотреть, что продаётся. А продаются китайские аккумуляторы с большим саморазрядом и ещё какими-то приколами. Так что 20 циклов реальность, а не «с потолка». В последнее время много подделок попадаются. Мало того — многого просто нет, потому что выпуск оригинальных товаров давно прекращён.
Так что рекомендованные 20 циклов — это наша реальность.
«реальность» что бы окончательно ушатать и пойти за новыми.
Эффект памяти у современных Ni-MH. Попытки обнаружения
Эффект памяти у современных Ni-MH аккумуляторов. Часть 2
Аккумуляторы LADDA ААА 900 mAh, 5.5 лет хранения без подзарядок + попытка обнаружения эффекта памяти
Вы знаете, я тот самый мифический эффект памяти на Ni-MH ловлю уже много лет. И никак не могу поймать. Что я не так делаю? ;)
~~~~~~~~~~~~~~~~~~~~
А самое смешное, что его и не должно быть, ибо никаких предпосылок с т.з. электрохимии нет от слова «совсем». Просто понять, что эффект памяти у Ni-Cd тупо связан Cd-электродом у некоторых мозгов не хватает (это не о вас, а о некоторых бравых электриках). А ведь электрода Cd(ОН)₂ у Ni-MH нет по определению.
Эффект памяти у Ni-MH придуман
клоунамибравыми электриками, которые тупо переносят все, что имело место быть в случае Ni-Cd на Ni-MH.Деградация электродов зависит от количества цикла заряда/разряда? Так вот у них даже 100 не было. У меня фотоаппарат от такого безумного количества заряда быстрее умер бы. 6 комплектов по 200 снимков (и даже если по 100), по 100 циклов. Фантастика для затвора. Единственный, который работал от AA. Мыльница с большим током потребления и довольно маленьким ресурсом затвора. Остальные фотоаппараты с LiPo. Сонькин LiPo с 2006, купленный б/у, правда, в Японии, сейчас имеет ёмкость больше номинальной.
Ну не знаю, наверное Ваш опыт и знания больше. Чего ж они тогда из полной дохлости частично восстанавливались?
На самом деле, inflexion и -∆V весьма близки. В одном случае левее, во втором — правее по кривой напряжения заряда.